Te pego na saída!
Publicado por Professor Igor Química em Uncategorized em fevereiro 19, 2012
Pimenta mais ardida do mundo é cultivada em Mirandópolis, SP
Nosso Campo – TV TEMQuem não gosta de uma pimenta, né?
Muitos dizem que elas ajudam no processo de emagrecimeto por acelerar o metabolisto, liberam endorfina – hormônio ligado ao prazer -, além de retardar o envelhecimento celular.
Bom, isso tudo é o que dizem… se é verdade eu já não sei. Mas sei que tem umas danadas que fazem muito marmanjo barbado chorar e pedir… pedir… seja lá o que for para para a sensação de ardor na boca.
O responsável por esta sensação muitas vezes desagradável é a capsaicina, compostos de fórmula molecular C18H27NO3 e estrutural mostrada abaixo
É irritante para mamíferos, incluindo humanos e causa sensação de queimação e ardor em contato com qualquer tecido.
E para passar a dor da pimenta nada melhor que um bom copão d’água, não é mesmo?
NÃO mesmo!
A capsaicina é um composto apolar, ou seja, hidrofóbico. A água só irá espalhar o composto por toda a boca, aumentando assim a tal queimação. É semelhante a tentar apagar com água o fogo numa panela contendo óleo de fritura – a água só irá espalhar o óleo e assim aumentar o incêndio!
Mas e ai, o que será que é bom para combater o “incêndio” da pimenta, hein?!
O café sem Ina!
Publicado por Professor Igor Química em Divulgação em fevereiro 6, 2012
Café descafeinado pode proteger o organismo contra diabetes tipo 2
Bebida é capaz de ativar metabolismo cerebral que é deficiente em diabéticos e em pessoas com problemas cognitivos
Revista Veja – Notícias: Nutrição
Um novo estudo desenvolvido na Faculdade de Medicina de Mount Sinai, nos Estados Unidos, indica que o café descafeinado é capaz de melhorar o metabolismo cerebral associado ao diabetes tipo 2. Essa ação do cérebro, se reduzida, também pode provocar problemas cognitivos. A pesquisa foi publicada na edição de janeiro do periódico online Nutritional Neuroscience.
Os resultados mostraram que os ratos, ao receberam o café sem cafeína, foram capazes de metabolizar a glicose de maneira mais eficaz, utilizando-a como fonte de energia para o cérebro e evitando que ela se acumulasse no organismo, provocando, ou piorando, o quadro do diabetes. Esse processo de uso da glicose é reduzida em pessoas com diabetes tipo 2 e, além dessa doença, pode acarretar diversos problemas cognitivos. “O metabolismo energético cerebral prejudicado está associado ao declínio cognitivo que ocorre com o envelhecimento do indivíduo e pode impulsionar o aparecimento de doenças neurodegenerativas mais sérias, como a Doença de Alzheimer”, diz Giulio Maria Pasinetti, coordenador do estudo.
A cafeína , assim como o quinino citado no post sobre malária – A Tônica da Maleita -,
é um alcaloide de fórmula molecular C8H10N4O2. Uma característica geral dos alcaloides é que se apresenta, em sua forma isolada, como um pó branco e amargo ao paladar. Atua como um estimulante do sistema nervoso central em humanos, sendo uma das drogas psicoativas mais utilizadas no mundo… e por sorte esta é legal pois muita gente por aí é viciado nela!
Acho que nem preciso comentar muito sobre os efeitos de uma bela xícara de café, não é mesmo? Todos sabem que ela dá aquele ânimo ao acordar e principalmente no meio da tarde quando já estamos com a bateria quase indo embora. Sem contar que o café em si é um ótimo atrativo social.
Mas não vá abusando da cafeína, pois ela pode tirar seu sono!
De acordo com o ministério da agricultura (http://www.agricultura.gov.br) o Brasil é o maior produtor mundial de café e o segundo país em consumo, sendo duas variedades de grãos as mais plantadas: Arábica e Conillon (Robusta). Minas Gerais lidera a posição de Estado produtor.
Bom, voltando ao assunto do café descafeinado.
Como é o processo de retirada da cafeína do café, hein?!
O processo de descafeinação é realizado com os grãos inteiros e ainda crus, ou seja, antes da torrefação, onde se utiliza um solvente que possui afinidade química com a cafeína (“semelhante dissolve semelhante”) e assim carrega-a para fora dos grãos. Os métodos existentes de descafeinação utilizam, em sua maioria, solventes orgânicos, principalmente o diclorometano – um halogenoalcano ou haloalcano – o mais utilizado no Brasil. Também temos o uso de clorofórmio (triclorometano), acetato de etila, álcool (etanol), acetona (propanona), água e o mais legal de todos: o CO2 supercrítico.
Segundo o professor Reinaldo Bazito – que foi meu professor na USP, diga-se de passagem, os fluidos supercríticos são:
Qualquer substância que foi pressurizada e aquecida acima de sua pressão e temperatura críticas(Ponto Crítico), passando a ter propriedades intermediárias entre um gás e um líquido. Eles difundem como gases e dissolvem outros materiais como líquidos, por exemplo.
O gráfico abaixo mostra um diagrama de fases para o CO2, indicando a região em que ele se encontra no estado supercrítico (73,8 bar e 31,0oC).
FUVEST 2012
Publicado por Professor Igor Química em Uncategorized em fevereiro 3, 2012
Confira abaixo a lista de aprovados na FUVEST 2012
Parabéns a todos os aprovados!
Força e determinação neste ano para aqueles que continuarão brigando!
A Tônica da Maleita
Publicado por Professor Igor Química em Uncategorized em fevereiro 3, 2012
Pesquisa nos EUA dobra número de mortes por malária no mundo
Doença causou mais de 1,2 milhão de mortes em 2010; OMS aponta 655 mil óbitos
Estadão – 03 de fevereiro de 2012 | 7h 44
A malária causou 1,2 milhão de mortes em 2010, quase o dobro do estimado no último relatório da Organização Mundial da Saúde (OMS), o que dificulta ainda mais o objetivo de erradicar esta doença até 2015.
Estes dados estão contidos em um estudo do Institute for Health Metrics and Evaluation (IHME) da Universidade de Washington que foi divulgado pela revista científica “The Lancet”.
Segundo a OMS, em 2010 houve 655 mil mortes por malária, que é transmitida pela picada de um mosquito, sendo que 91% dos casos ocorreram na África e 86% tiveram como vítimas crianças com menos de cinco anos.
A malária, também conhecida como:
- Maleita
- Paludismo ou Impaludismo
- Febre palustre
- Febre dos pântanos
- Febre negra
- Febre intermitente
- Febre terçã ou sezão
- Febre quartã
É causada por um protozoário: Plasmodium sp.
Os protozoários são organismos microscópicos, unicelulares e heterótrofos, sendo suas funções – nutrição, excreção, respiração, reprodução – são realizadas por uma única célula. São divididos em grupos como os Rizópodes, Flagelados, Ciliados e Esporozoários.
Os plasmódios (sim, são mais de dois tipos) causadores da malária pertencem ao grupo dos esporozoários, parasitos que não apresentam estruturas de locomoção; sua reprodução ocorre pela processo de esporulação: reprodução assexuada que tem a capacidade de gerar muitos indivíduos descendentes de uma única vez – os esporos.
Podem causar a malária as seguintes espécies de Plasmodim:
- Plasmodium vivax
- Plasmodium falciparum
- Plasmodum malarie
- Plasmodium ovale
A transmissão da malária é dada pela picada apenas das fêmeas de cerca de cinquenta espécies de mosquitos do gênero conhecido como Anopheles (mosquito prego), parecidos com pernilongos, que é o hospedeiro definitivo, pois nele o parasito se reproduz sexuadamente. Também pode ser transmitida por transfusão de sangue contaminado, através da placenta (congênita) para o feto e por meio de seringas infectadas.
Ciclo do parasita
O plasmódio desenvolve um ciclo sexuado dentro do organismo do mosquito e um assexuado no organismo humano. Depois de 30 minutos que entrou na circulação sanguínea do homem, alcança o fígado e vai-se multiplicando dentro das células hepáticas até que elas arrebentam. Então, eles se espalham no sangue e invadem os glóbulos vermelhos, onde se reproduzem a tal ponto que eles se rompem também.
Sintomas
Os sintomas mais comuns são febre alta, calafrios intensos que se alternam com ondas de calor e sudorese abundante, dor de cabeça e no corpo, falta de apetite, pele amarelada e cansaço. Dependendo do tipo de malária, esses sintomas se repetem a cada dois ou três dias.
Não há uma vacina contra a malária, mas alguns compostos orgânicos fazem parte do tratamento farmacológico de pacientes contaminados.
O primeiro composto utilizado no tratamento da malária foi o quinino (C20H24N2O2), um alcaloide extraído da cinchona. O termo alcalóide significa “semelhente a alcalis”. Esse termo é dado a está classe de composos orgânicos pois estes possuem características básicas – bases de Lewis – devido a presença de pares eletrônicos livres dos átomos de nitrogênio. *Saiba mais sobre outras definições de ácidos e bases.
o quinino é encontrado na água tônica e é o responsável pelo sabor amargo característico da bebida que só é suportável ao paladar para pessoas acima de certa idade.
o quinino é derivado da quinolina, um composto heterocíclico aromático, também extraído da cinchona.
também são derivados da quinolina outros compostos com ação antimalárica, como por exemplo, o cloroquina.
o problema da cloroquina está relacionada com sua toxicidade que pode causar retinite e até cegueira.
Muitos estudos são feitos em busca de novos tratamento para o combate a malária. Além de ser uma infecção difícil de ser tratada devido à esperteza do parasito, a malária é uma doença de “terceiro” mundo que acaba sendo negligenciada por grande empresas farmacêuticas.
To regulando no açúcar!
Publicado por Professor Igor Química em Divulgação em fevereiro 2, 2012
Consumo de açúcar deve ser regulado, afirmam cientistas
Novo estudo indica que os efeitos danosos do açúcar no organismo são semelhantes aos promovidos pelo álcool; diabetes está entre as doenças que mais causam mortes
Em comentário publicado na edição desta quinta-feira, 2, da revista Nature, três cientistas da Universidade da Califórnia em San Francisco destacam outro responsável pela mudança na saúde pública mundial, além do cigarro e do álcool: o açúcar.
Os autores afirmam que os efeitos danosos do açúcar no organismo humano são semelhantes aos promovidos pelo álcool e que seu consumo também deveria ser regulado.
Estadão – Saúde: 02 de Fevereiro de 2012
Acho que não era tão necessário assim ter três cientistas e um artigo na Nature para saber que o açúcar – em excesso – não é lá muito bom para saúde, não! Se bem que qualquer coisa em excesso não é um bom negócio, não é mesmo?
Nosso organismo, assim como carro, necessita diariamente de certa quantidade de energia. Esta é provida em grande parte pelos carboidratos (também conhecidos como sacarídeos – do Grego: sakcharon, açúcar), uma classe de compostos orgânicos. É interessante notar que todos os carboidratos ou hidratos de carbono possuem entre si uma semelhança que é a molécula de glicose. Nosso metabolismo, ou melhor, o conjunto de reações químicas que ocorrem no organismo, quebram os carboidratos resultando em glicose – um monossacarídeo, uma molécula de açúcar simples – que percorre nosso corpo através do sangue, provendo assim energia para todas as células.
Duas moléculas de açúcar simples podem se ligar entre si formando uma “molécula dupla”.
O terrível açúcar de mesa que adoça nossa vida, nada mais é que uma dessas moléculas duplas formadas por uma molécula de glicose mais uma de frutose, sendo também chamada de dissacarídeo.
Outros dissacarídeos importantes são a lactose (glicose + galactose) açúcar encontrado no leite e maltose (glicose + glicose), também conhecido como açúcar do malte.
Bom, voltando ao temido açúcar de mesa que é tão ou mais prejudicial que o álcool ou o tabaco, aqui no Brasil ele é fabricado a partir do caldo de cana-de-açúcar. Já na Europa o açúcar é feito de beterrabas por um processo bem semelhante ao da cana. O problema é que dizem que a caipirinha feita com açúcar de beterraba não fica tão legal, não… mesmo com uma boa cachaça mineira!
E esse tal de açúcar invertido, o que é que ele é?
Quando se faz passar uma luz especial (luz plano polarizada) por uma solução de sacarose, percebe-se que esta tem a capacidade de rotacionar, mudar, a direção da propagação do plano da luz no sentido horário. Quando a água quebra a molécula do dissacarídeo num processo que chamamos carinhosamente de hidrólise com o auxílio de enzimas – as invertases –, a solução resultante rotaciona esta mesma luz especial no sentido contrário, ou seja, anti-horário. É por isso que chamamos o açúcar de invertido, pois agora ele inverte a rotação “original” da luz!
E o que tem de tão especial nesse açúcar?
Ele é mais doce que o próprio açúcar!
Pois é… mais doce ainda pois agora temos a presença de frutose livre na mistura. A frutose é mais doce em relação à sacarose cerca de 33% (!) sendo encontrada em muitos alimentos industrializados.
Mas não se preocupe, pois a frutose libera as mesmas 4 kcal (quilocalorias) por grama que a sacarose.
Segue um video sobre sacarose:
Quatro morrem intoxicados em curtume em Mato Grosso do Sul
Publicado por Professor Igor Química em Uncategorized em fevereiro 1, 2012
Quatro pessoas morreram e 16 foram hospitalizadas com intoxicação após a liberação de uma massa de gás ácida em acidente ocorrido no curtume de propriedade do frigorífico Marfrig, em Bataguassu (MS). Dos 16 sobreviventes, três foram levados para um hospital em Presidente Prudente (SP).
Folha de São Paulo (Cotidiano) – Acesso 31/ Janeiro/ 2012
O Sulfidrato de Sódio (NaHS) é um agente redutor utilizado no processo de depilação/ caleiro no processo de curtume de peles animais (transformação de pele em couro).
O Sulfidrato de sódio é obtido pela neutralização parcial do ácido sulfídrico (H2S) com compostos básicos, por exemplo, o hidróxido de sódio (NaOH).
Entretanto, o sulfidrato de sódio em meio ácido pode gerar o gás sulfídrico que além de possuir um desagradável cheiro de ovos podres, é altamente tóxido e irritante às vias aéreas superiores e pulmão.
NaHS + H+ (ácido) → H2S + Na+
Uhn, que gosto azedo… E que cheiro!
Publicado por Professor Igor Química em Divulgação em janeiro 4, 2012
Bom, continuando o nosso estudo sobre ácidos, hoje vamos ver um pouquinho sobre os Ácidos carboxílicos.
Estes compostos são praticamente onipresentes nos vestibulares, então é bom ficar de olho!
Bora lá, galera…
De onde vem o cheiro forte do vinagre? E o seu sabor azedo, de onde vem? Será que estão relacionados um ao outro?
As respotas para estas perguntas está na presença de um ácido contido no vinagre, conhecido como ácido acético (acetum – do latim – e vin aigre – do francês – significam “vinho azedo”).
O ácido acético é o nome usual do ácido etanóico, um composto pertencente a uma classe de compostos orgânicos conhecidos como ácidos carboxílicos. Essa classe de compostos é representada pela presença do grupo funcional carboxíla:
A nomenclatura oficial dos ácidos carboxílicos, segundo a IUPAC, é formada pela palavra ácido seguida pelo nome do alcano modificado pela terminação –óico. Vamos a alguns exemplos:
Estes compostos são polares e de alto ponto de ebulição. Isto ocorre devido à presença de duas pontes ou ligações de hidrogênio entre as carboxílas nos estados sólido e líquido.
Os ácidos de cadeia pequena (até quatro átomos de carbono) são solúveis em água, ou seja, em solventes polares, apresentando uma diminuição de solubilidade com o aumento da cadeia de carbonos.
Em relação ao odor daqueles que são voláteis, não são nada agradáveis. Vale lembrar o cheiro que tem o vinagre! A presença, por exemplo, do ácido butanoico (ácido butírico) na manteiga rançosa é a causa do cheiro característico, além de dar cheiro a muitos queijos.
Em 1991, o ácido 3-metil-2-hexenóico (ou 3-metil-hex-2-enóico) foi identificado como sendo o principal responsável pelo odor do suor humano, bem conhecido daqueles que se utilizam do transporte coletivo lá pelas seis horas da tarde. Eu sei que você sabe bem do que estou falando… só não sabia que era um ácido carboxílico, não é mesmo?
Os ácidos carboxílicos de cadeia longa, ou seja, cadeias superiores a 11 átomos de carbono, sem contar o carbono da carboxíla, formam uma classe importante destas ácidos e são chamados de ácidos graxos, cujo nome deriva de sua fonte, as gorduras naturais.
*Os nomes comuns – não usuais – dos ácidos carboxílicos foram dados para descrever alguma característica do composto ou sua fonte de origem.
Ácido fórmico (metanoico) – presente nas formigas vermelhas e isoladas através da destilação destrutivas das “bixinhas”com vapor d’água; também presente nas urticarias. É responsável pela sensação de ardência e coceira quando da picada de uma formiga.
Ácido acético (etanóico) – componente do vinagre (não é o vinagre em sí, hein?!) acetum = vinagre.
Ácido butírico (butanoico) – presente no ranço da manteiga – do inglês, butter.
Ácidos capróico (hexanóico) e caprílico (octanóico) – odor de cabra – do latim, caper.
Ácidos carboxílicos de ocorrência natural
Ácido Pirúvico: Produto da metabolização da glicose
Ácido Láctico: Responsável pela sensação de queimação nos músculos durante exercícios físicos intensos com déficit de oxigênio, sendo também encontrado no leite azedo.
Ácido Oxálico: O famoso “azedinho” é encontrado em vegetais de folhas verdes e também no tomate; forma compostos pouco solúveis em presença de íons Ca2+, sendo esta uma das causas de pedras nos rins.
Para os próximos posts, vamos ver como ocorre a síntese dos ácidos carboxílicos! Até lá…
… mas antes, segue um exercío da FUVEST 2011:
(Fuvest 2011) Um sólido branco apresenta as seguintes propriedades:
I. É solúvel em água.
II. Sua solução aquosa é condutora de corrente elétrica.
III. Quando puro, o sólido não conduz corrente elétrica.
IV. Quando fundido, o líquido puro resultante não conduz corrente elétrica.
Considerando essas informações, o sólido em questão pode ser
a) sulfato de potássio.
b) hidróxido de bário.
c) platina.
d) ácido cis-butenodioico.
e) polietileno.
Vídeo-aulas de vestibular do portal G1, confiram!
Uhn, mas que gosto azedo!
Publicado por Professor Igor Química em Divulgação em dezembro 29, 2011
Teoria de Ácidos e Bases
Antes de uma sistematização química do que eram substâncias ácidas e básicas, os químicos consideravam como sendo ácidos todas as substâncias que possuíssem saber azedo. Aliás, a palavra ácido vem do latim acidus, que justamente significa azedo. Alguns ácidos são bem familiares no nosso cotidiano, como por exemplo, o ácido cítrico que é encontrado no limão além de outras frutas cítricas; o ácido acético ou etanóico, componente do vinagre; e também o ácido clorídrico (HCl) encontrado no estômago e associado ao sabor azedo do vômito. Outras características destas substâncias são a de tornar vermelho o tornassol e reagir com certos metais com liberação de gás hidrogênio (H2)
Compostos que possuíam a capacidade de neutralizar um ácido, como as cinzas de madeira e outras plantas, eram chamadas de bases ou compostos alcalinos – cinza em Árabe é al kalai. Podemos falar também que as bases provocam uma sensação escorregadia quando em contato com as mãos, deixar o tornassol azul e ter um gosto adstringente.
Percebe-se que os métodos de saber se uma substância é ácida ou básica pelo sabor azedo ou pela sensação atribuída quando esfregada nas mãos não é nada seguro, podendo causar graves danos à saúde, ou seja, as definições fenomenológicas nestes casos não são válidas.
Foi em somente 1887 (perceba que são apenas 124 anos considerando 2011) que o químico e físico Sueco Svante August Arrhenius propôs que toda e qualquer substância que gerasse íons H+ em água era um ácido e que aquelas que gerassem íons OH– em água, eram bases.
Ácidos – Segundo Arrhenius, Substâncias que geram H+ em água
Bases – Segundo Arrhenius, Substâncias que geram OH– (hidroxila) em água
Mesmo sendo muito boa e resolvendo grande parte da nossa vida, a definição de Arrhenius se mostrou muito limitada uma vez que muita química acontece na total ausência de água.
Foi pensando nisso que em 1923, o químico dinamarquês Johannes Bronsted e o inglês Thomas M. Lowry, definiram de forma independente, que ácidos são substâncias que transferem prótons (H+) e bases são substâncias que recebem prótons. A água pode ser o solvente, mas não há necessidade para esta definição.
Ácidos e Bases de Bronsted-Lowry
Ácidos: doadores de prótons, íons H+ / Bases: aceptores de prótons, íons H+
Bom, mas essa conversa de ácidos e bases ainda não terminou.
Uma terceira definição, agora muito mais generalista, foi cunhada pelo químico Gilbert N. Lewis, aquele mesmo que vocês adoram das estruturas eletrônicas, onde os elétrons são bolinhas!
Pois bem, Lewis defini um ácido como sendo um composto que pode aceitar um par de elétrons e uma base com doadora de pares de elétrons.
Para registrar um exercício provando que isso vem sendo cobrado nos vestibulares, segue uma questão da UNESP 2011 vestibular de inverno:
(UNESP 2011) A sibutramina, cuja estrutura está representada, é um fármaco indicado para o tratamento da obesidade e seu uso deve estar associado a uma dieta e exercícios físicos.
(A) é uma base de Lewis, porque possui um átomo de nitrogênio que pode doar um par de elétrons para ácidos.
(B) é um ácido de Brönsted-Lowry, porque possui um átomo de nitrogênio terciário.
(C) é um ácido de Lewis, porque possui um átomo de nitrogênio capaz de receber um par de elétrons de um ácido.
(D) é um ácido de Arrhenius, porque possui um átomo de nitrogênio capaz de doar próton.
(E) é uma base de Lewis, porque possui um átomo de nitrogênio que pode receber um par de elétrons de um ácido.
Confira abaixo uma Vídeo-aula resumindo as definições de ácidos e bases
Confira também ácidez e basicidade: https://igorsuga.wordpress.com/2011/11/09/197/
Ih, Vazou! [2]
Publicado por Professor Igor Química em Divulgação em novembro 17, 2011
Chevron concede entrevista ao blog da Miriam Leitão sobre o vazamento de petróleo na Bacia de Campos, RJ.
Confira a entrevista no blog:
Chevron fala ao blog sobre vazamento de óleo – – Míriam Leitão – O Globo.
Segue abaixo também o blog Sky Truth, mantido pelo geógrafo John Amos, especializado em interpretação de fotos de satélite, indicando que o vazamento pode ser dez vezes maior que o estimado.
http://blog.skytruth.org/2011/11/chevron-oil-spill-off-brazil-10-times.html
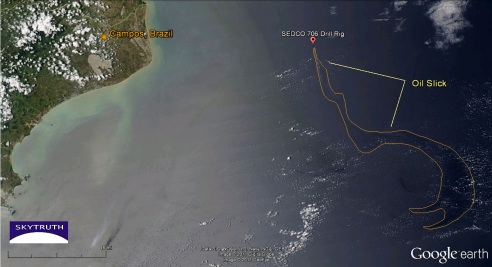
Imagem de Satélite mostra a mancha de óleo.




















